“Molecule of the Week” layihəsi çərçivəsində Günel Əzimova tərəfindən yazılan məqalə: “Eykosapentaen Turşusu”.
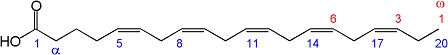
5,8,11,14,17-Eykosapentaen turşusunun xətti quruluşu CH3(CH2CH=CH)5(CH2)3CO2H kimidir. Molekulyar çəkisi 302,45 q/mol-dur. Bioloji mənbəyi balıq yağıdır. Rəngsiz maye formasındadır. Metanolda həll olur. Ampulada 10, 25, 50, 100 mq olur.
Eykosapentaen turşusu (EPA) həm də ikosapentaen turşusu adlanır. Omeqa-3 tərkibli yağ turşusudur. Fizioloji ədəbiyyatda ona 20:5(n-3) adı verilib. Trivial adı timnodon turşusu adlanır. Kimyəvi quruluşunda EPA 20 karbonlu zəncir və beş sis ikiqat rabitəsi olan karboksilik turşudur. İlk ikiqat rabitə omeqa ucundan 3-cü karbonda yerləşir. EPA prostaqlandin-3 (trombositlərin yığılmasına maneə törədən), tromboksan-3 və leykotrien-5 eykosanoidlərinin prekursoru kimi özünü göstərən doymamış yağ turşusudur (PUFA). EPA eykosapentaenoil etanolamidin həm prekursor, həm də parçalanma məhsuludur. EPA yağlı balıq yeməklə qəbul edilir. Həmçinin insan südündə də tapılmışdır. Eykosapentaen turşusu adətən bitkilərdə olmur. İnsan bədəni udulmuş alfa-linolen turşusunun bir hissəsini EPA-ya çevirir. Alfa-linolen turşusu əsas yağ turşusudur. Bununla belə alfa-linolen turşusunun EPA-ya çevrilməsinin səmərəliliyi, EPA-nın tərkibində olan qidanın udulmasından xeyli aşağıdır.
Eykosapentaen turşusu doymamış yağ turşusudur (PUFAs) və linolen turşusundan sintez olunur. Hüceyrə membranının fosfolipid bilayerlərində, beynin sinaptik membranlarında və tor qişada paylanır. Əsasən balıq yağı, dəniz yosunu, fitoplankton və dəvədən əldə edilir. Omeqa-3 yağ turşusu olmaqla, sis-trans konformasiyalarını göstərir.
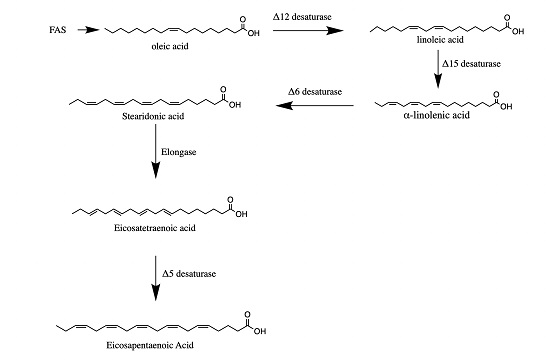
Prokariot və eukariotlarda eykosapentaen turşusunun biosintezinə poliketid sintaza daxildir. Poliketid sintazaya 6 ferment daxildir: 3-ketoasil sintaza, 2-ketoasil sintaza-ACP-reduktaza, dehidraza, enoil reduktaza, dehidrataza/2 trans 3-kos izomeraza, dehidrataza/2 trans və 2-sis izomeraza. EPA-nın biosintezi dəniz növlərində dəyişir, lakin dəniz növlərinin əksəriyyəti C18 PUFA-nı LC PUFA-ya çevirir, bu da yağlı asil dezaturaza və elonqaza fermentlərindən asılıdır. Fermentlərin molekul əsası yaranan molekul əsasında ikiqat rabitənin harada əmələ gəldiyini göstərir. Aşağıda yağ turşusu sintezindən EPA-nın biosintezinin ümumi görünüşü verilib. Reaksiyalar x spesifikliyi olan dezaturaza fermenti ilə nəhayətlənir və yağ turşusu zəncirlərinin uzanması ilə uzanır:
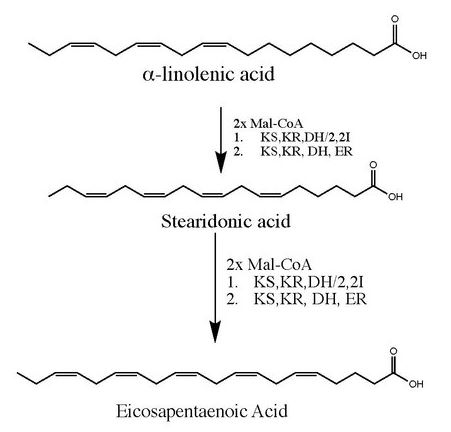
Şevanellada EPA-nın təklif olunmuş poliketid sintez yolu reduksiya, dehidratlaşma, kondensləşmə reaksiyasının təkrar reaksiyasıdır. α-linolen turşusunun EPA-ya çevrilmə mexanizmi KS tərəfindən malonil-CoA-nın əvvəlcədən mövcud olan α-linolen turşusuna kondensasiyasını əhatə edir. Nəticədə quruluş NADPH-dən asılı reduktaza, KR tərəfindən DH fermenti tərəfindən susuzlaşdırılan bir aralıq məhsula çevrilir. Son mərhələ ER fermenti aktivliyi vasitəsilə trans-2-enoli-ACP-də ikiqat rabitənin NADPH-dən asılı olaraq reduksiyasıdır. EPA alınması üçün proses təkrarlanır.
Tibbi əhəmiyyəti: ABŞ Milli Sağlamlıq İnstitutunda eykosapentaen turşusu səmərəli müalicə üsulu kimi tanınır. Bunların əksəriyyəti iltihab müalicəsində istifadə olunur. Görünür ki, həm EPA, həm də DHA daha aşağı triqliseridlərdir, lakin DHA aşağı sıxlıqlı lipoproteinləri yüksəldir. EPA və DHA etil efirləri (bütün formalar) acqarına və ya az yağlı yeməklə qəbul edildikdə daha az yaxşı absorbsiya olunur, beləliklə, daha az işləyir. Omeqa-3 yağ turşuları, xüsusən də EPA otistik spektr pozğunluğunun qarşısının alınmasında geniş istifadə olunmuşdur.
Tətbiqi:
- Hepatositlərdə steatoza farmakoloji təsirini yoxlamaq;
- İnsanda döş xərçəngi nümunələrini xarakterizə etmək üçün Raman spektrlərinin ölçülməsində analitik standart kimi;
- Siçan embrion fibroblastlarında lipid peroksidləşmə analizində və hüceyrə canlılığının tədqiqatları üçün hüceyrələrin ilkin müalicəsində geniş istifadə edilir.
Eykosapentaen turşusu (EPA) sağlam həyat üçün vacibdir və piylənməni azaldır. Bundan başqa çox aşağı sıxlıqlı lipoprotein (VLDL) səviyyələrini modulyasiya edərək triqliserid səviyyələrini azaldır.
Ədəbiyyat:
- Monroig, Óscar; Tocher, Douglas; Navarro, Juan (2013-10-21). “Biosynthesis of Polyunsaturated Fatty Acids in Marine Invertebrates: Recent Advances in Molecular Mechanisms” Marine Drugs. 11 (10): 3998–4018. doi:10.3390/md11103998
- Halliday J (12 January 2007). “Water 4 to introduce algae DHA/EPA as food ingredient”. Retrieved 2007-02-09.
- Simopoulos AP (2002). “Omega-3 fatty acids in wild plants, nuts and seeds”. Asia Pacific Journal of Clinical Nutrition. 11 (Suppl 2): S163–73. doi:10.1046/j.1440-6047.11.s.6.5.x
- Moi, Ibrahim Musa; Leow, Adam Thean Chor; Ali, Mohd Shukuri Mohamad; Rahman, Raja Noor Zaliha Raja Abd.; Salleh, Abu Bakar; Sabri, Suriana (July 2018). “Polyunsaturated fatty acids in marine bacteria and strategies to enhance their production”. Applied Microbiology and Biotechnology. 102(14): 5811–5826. doi:1007/s00253-018-9063-9
- Ilardi, Stephen. “Therapeutic Lifestyle Change. A new treatment for depression”. Therapeutic Lifestyle Change (TLC). Retrieved 9 November 2019. We were never designed for the sedentary, indoor, sleep-deprived, socially-isolated, fast-food-laden, frenetic pace of modern life.
- Mankad D, Dupuis A, Smile S, Roberts W, Brian J, Lui T, Genore L, Zaghloul D, Iaboni A, Marcon PM, Anagnostou E (2015-03-21). “A randomized, placebo controlled trial of omega-3 fatty acids in the treatment of young children with autism”. Molecular Autism. 6: 18. doi:10.1186/s13229-015-0010-7
- Che-Hsin Lee, Shin-Da Lee, Hsiu-Chung Ou, Su-Chuan Lai, Yu-Jung Cheng. Eicosapentaenoic acid protects against palmitic acid-induced endothelial dysfunction via activation of the AMPK/eNOS pathway. International journal of molecular sciences (2014-06-12).
- Hsueh TY, et al. Effect of eicosapentaenoic acid and docosahexaenoic acid on myogenesis and mitochondrial biosynthesis during murine skeletal muscle cell differentiation. Frontiers in nutrition, 5, 15-15 (2018)
- Cholewski M, et al. A Comprehensive Review of Chemistry, Sources and Bioavailability of Omega-3 Fatty Acids. Nutrients, 10(11), 1662-1662 (2018)
- MatsHamberg. Transformations of 5,8,11,14,17-eicosapentaenoic acid in human platelets. Biochimica et Biophysica Acta (BBA) – Lipids and Lipid Metabolism. Volume 618, Issue 3, 23 June 1980, Pages 389-398
- Friedrich Jüttner. LIBERATION OF 5,8,11,14,17-EICOSAPENTAENOIC ACID AND OTHER POLYUNSATURATED FATTY ACIDS FROM LIPIDS AS A GRAZER DEFENSE REACTION IN EPILITHIC DIATOM BIOFILMS. Journal of Phycology. Volume 37, Issue 5 p. 744-755
- Sato M, Imada K, Iida S, Ohashi K, Yamaguchi K, Kosuzume H, Shibutani Y, Kunihiro Y. [General pharmacological studies on 5,8,11,14,17-eicosapentaenoic acid ethyl ester (EPA-E)]. Nihon Yakurigaku zasshi. Folia Pharmacologica Japonica, 01 Jul 1989, 94(1):35-47
- MikeVanRollins, Peter D.Frade, Oscar A.Carretero. Oxidation of 5,8,11,14,17-eicosapentaenoic acid by hepatic and renal microsomes. Biochimica et Biophysica Acta (BBA) – General Subjects Volume 966, Issue 1, 14 July 1988, Pages 133-149
- H. Juan,B.A. Peskar,Th. Simmet. Effect of exogenous 5, 8, 11, 14, 17-eicosapentaenoic acid on cardiac anaphylaxis. First published: February 1987. https://doi.org/10.1111/j.1476-5381.1987.tb08961.x
- J.Dyerberg, K.A.Jørgensen, T.Arnfred. Human umbilical blood vessel converts all cis 5,8,11,14, 17 eicosapentaenoic acid to prostaglandin I3. Prostaglandins Volume 22, Issue 6, December 1981, Pages 857-862
- Teresa WilhelmWeiner, HowardSprecher. Arachidonic acid, 5,8,11-eicosatrienoic acid and 5,8,11,14,17-eicosapentaenoic acid: Dietary manipulation of the levels of these acids in rat liver and platelet phospholipids and their incorporation into human platelet lipids. Biochimica et Biophysica Acta (BBA) – Lipids and Lipid Metabolism Volume 792, Issue 3, 7 March 1984, Pages 293-303
- Wikipedia