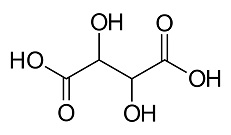
“Molecule of the Week” layihəsi çərçivəsində Nəzrin Qasımova tərəfindən yazılan məqalə: “L-(+) Çaxır Turşusu”.
Ümumi formulu: C4H6O6 COOH(CHOH)2COOH
Çaxır turşusu-2 əsaslı 4 atomlu oksiturşuların daha çox istifadə olunan nümayəndəsi dioksikəhrəba və ya çaxır (tartarat) turşusudur. Bütün oksiturşuların kəşfi isveç alimi Karl Şeyelenin adı ilə bağlıdır. Onun kəşfi 1769-1785-ci illəri əhatə edir. İlk dəfə o, çaxır turşusunu kəşf etmişdir.
Çaxır turşusu təbii olaraq bir çox meyvələrdə, xüsusən üzümdə, banan və sitrus meyvələrində yaranan ağ rəngli, kristal üzvi turşudur. Natrium bikarbonat ilə qarışdırılır və qida hazırlanmasında maya kimi istifadə olunan qabartma tozu kimi satılır. Turşunun özü qidalara antioksidant E334 olaraq əlavə olunur və fərqli turş dadı verir.
Fiziki xassələri: Çaxır turşusu qoxusuz, ağ rəngli toz halında olan hiqroskopik maddədir. Turşuda, suda və etil spirtində, benzolda, efirdə, karbohidrogenlərdə həll olmur. Ərimə temperaturu 170-206 °C aralığındadır.
I və II formullar enantiomerlərdir. Enantiomerlərin bərabər miqdarda qarışığı rasemat adlanır. Rasematlar optiki qeyri-fəal olurlar. Mezoçaxır turşusunun III və IV formulları eyni bir maddə olduqlarına görə enantiomerlər deyillər. İki xiral mərkəzli molekulların D- və yaxud L- sıraya aid olması yuxarıdan birinci xiral karbon atomuna görə müəyyən edilir. Həmin xiral mərkəzdə funksional qrup sağda yerləşdikdə D-izomer, solda olduqda isə L- izomer olur. Mezoçaxır turşusunun molekulunda iki xiral mərkəzdən biri D-, digəri isə L-konfiqurasiyaya malik olmaqla, molekuldaxili rasemat əmələ gətirir. Ona görə də mezoçaxır turşusunun molekulu axiraldır və optiki qeyri-fəaldır. Tərkibində ikidən çox xiral mərkəz olan molekullarda D- və L- izomer əsas funksional qrupdan (monosaxaridlərdə karbonil qrupundan) ən uzaqda yerləşən xiral karbona görə və yuxarıda qeyd edilənlərə müvafiq olaraq müəyyən olunur.
Təbii olaraq meydana gələn çaxır turşusu üzvi kimyəvi sintezdə faydalı bir xammaldır. Turşunun təbii olaraq meydana gələn forması L-(+) çaxır turşusudur. Təbii olaraq mövcud olduğu üçün enantiomerindən və mezo izomerindən bir qədər münasib və əlverişlidir.
Alınması:
L-(+) Çaxır turşusu. Çaxır turşusunun L-(+)-çaxır turşusu izomeri sənaye baxımından çox miqdarda istehsal olunur. Fermentasiyanın bərk əlavə məhsulundan əldə edilir. Əlavə məhsullar əsasən kalium bitartaratdan (KHC4H4O6) ibarətdir. Bu kalium duzu, əhəng südü (Ca(OH)2) ilə təsir edildikdə kalsium tartratına (CaC4H4O6) çevrilir:
KO2CCH(OH)CH(OH)CO2H + Ca(OH)2 → Ca(O2CCH(OH)CH(OH)CO2) + KOH + H2O
Praktikada kalsium xlorid əlavə edilərək daha yüksək miqdarda kalsium tartaratı əldə edilir. Daha sonra sulfat turşusu ilə işlənərək kalsium tartarat mezoçaxır turşusuna çevrilir:
Ca(O2CCH(OH)CH(OH)CO2) + H2SO4 → HO2CCH(OH)CH(OH)CO2H + CaSO4
Rasemik mezoçaxır turşusu (yəni: 50:50 nisbətində D-(-)-tartarat turşusu və L-(+)-tartarat turşu molekulları, rasemik turşu), malein turşusundan çox mərhələli reaksiya ilə hazırlana bilər. İlk mərhələdə malein turşusu katalizator olaraq kalium volfram istifadə edərək hidrogen peroksidlə epoksidləşir:
HO2CC2H2CO2H + H2O2 → OC2H2(CO2H) 2
Növbəti mərhələdə epoksid hidroliz edilir:
OC2H2(CO2H)2 + H2O → (HOCH)2(CO2H)2
Çaxır tuşusu şərabda: Şərab içənlər çaxır turşusunu şüşənin mantarında və ya dibində kortəbii olaraq əmələ gələn kiçik kalium bitartarat kristallarının, başqa sözlə “şərab almazlarının” mənbəyi kimi tanıyır. Bu “tartaratlar” zərərsizdir, baxmayaraq ki, bəzən şüşə sınması ilə səhv salınır və bir çox şərabda soyuq sabitləşdirmə yolu ilə qarşısı alınır. Çaxır turşusu kimyəvi cəhətdən əhəmiyyətli rol oynayır, mayalanma pH-ı bir çox arzuolunmaz bakteriyaların yaşaya bilməyəcəyi səviyyəyə endirir və mayalanmadan sonra qoruyucu rolunu oynayır. Çaxır turşusu limon və digər turşularla birlikdə ağızda şərabın bir qədər sərtliyini təmin edir. Araşdırmalar göstərir ki, bir çox sitrus meyvələrinin təkibində çaxır turşusu özünü ehtiva edir.
Tətbiqi : Çaxır turşusu və onun törəmələri əczaçılıq sahəsində bir çox istifadəyə malikdir. Məsələn, dərmanların dadını yaxşılaşdırmaq üçün limon turşusu ilə birlikdə bəzi duzların istehsalında istifadə edilmişdir.
Çaxır turşusunun sənaye istifadəsi üçün bir neçə tətbiqi də var. Turşunun kalsium və maqnezium kimi metal ionlarını şelatladığı müşahidə edilmişdir. Buna görə də, turşu əkinçilik və metal sənayesində torpaq gübrəsində mikroelementlərin kompleksləşdirilməsi və alüminium, mis, dəmir və bu metalların ərintilərindən ibarət metal səthlərin təmizlənməsi üçün şelatlaşdırıcı vasitə kimi xidmət etmişdir.
Ədəbiyyat:
- https://en.m.wikipedia.org/wiki/Tartaric_acid
- https://pubchem.ncbi.nlm.nih.gov/compound/Tartaric-acid
- https://www.sciencedirect.com/topics/medicine-and-dentistry/tartaric-acid
- https://www.britannica.com/science/tartaric-acid
- https://pubs.acs.org/doi/10.1021/ja01333a505