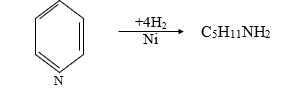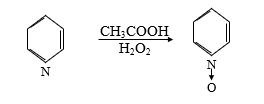“Molecule of the Week” layihəsi çərçivəsində Xəyalə Kəsəmənli tərəfindən yazılan məqalə: “Piridin”.
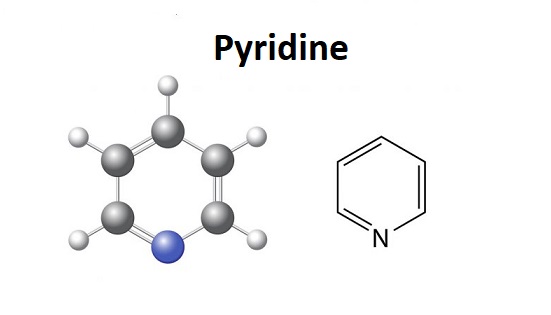
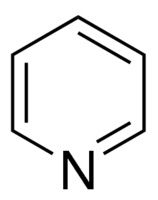
Piridin – C5H5N kimyəvi formuluna malik heterotsiklik üzvi birləşmədir. Piridin 115,4 0C-də qaynayan, spesifik iy verən, su ilə hər nisbətdə qarışan mayedir. Yanıcıdır və rəngsizdir. Piridin həlqəsi bir çox vacib birləşmələrdə – vitaminlərdə, dərman preparatlarında və aqrokimyəvi maddələrin tərkibində olur. Tarixən, piridin daş kömür qatranından, ağacın, torfun və sümüyün quru distilləsindən alınır. 2016-cı ildən dünya miqyasında ildə təxminən 20000 ton miqdarında sintez edilmişdir.
Piridinə benzoldakı üç valentli CH qrupunun azot atomu ilə əvəzlənmiş törəməsi kimi də baxmaq olar.
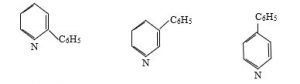
Quruluş nəzəriyyəsinə uyğun olaraq piridinin üç monoəvəzli və altı və ya on iki diəvəzli ola bilər ki, bu da əvəzedicilərin eyni və ya müxtəlif olmasından asılıdır.
Monometilpiridin pikolin, dimteilpiridin lutidin, trimetilpiridin isə kollidin adlanır.
Alınma üsulları: Piridini ilk dəfə sümük yağından (1851), sonra daş kömür qətranından (1854) ayırmışlar. 1850-ci ilə qədər daş kömür qətranı piridinin alınmasında sənayedə yeganə mənbə rolunu oynayırdı, halbuki qətranda onun miqdarı 0,1% təşkil edirdi.
Hazırda daş kömür qətranından ayrılan piridin və onun homoloqları sənayenin tələbatını ödəmək iqtidarında deyildir.
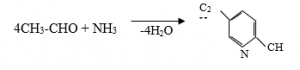
Piridin və onun homoloqlarının sintezi üçün bir sıra reaksiyalar irəli sürülmüşdür. Bunlardan ən əsası karbonil birləşmələrin ammonyakla kondensləşməsinə əsaslanır.
- Akrolein ammonyakla kondensləşməsi zamanı β-pikolin əmələ gətirir:
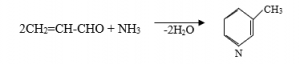
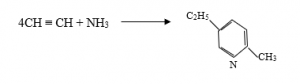
3. Mürəkkəb nikel və ya kobalt katalizatoru iştirakı ilə asetilen və ammonyakdan 2-metil-5-etilpiridin alınır (Reppe):
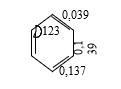
Fiziki xassələri: Piridin və onun yaxın homoloqları pis iyli, rəngsiz mayedirlər, suda həll olurlar. Piridin və benzolun quruluş oxşarlıqları elektron difraksiyalarının ölçülməsi nəticəsində bir daha təsdiq olundu. Məlum oldu ki, piridin həlqəsi demək olar ki, düzgün altıbucaqlıdır (rabitələrin uzunluğu nm-lə göstərilir):
Piridin və benzolun ultrabənövşəyi spektrləri çox oxşardır, benzoldan fərqli olaraq piridinin dipol momenti yüksəkdir (2,2D).
Kimyəvi xassələri: Piridin özünəbirləşdirmə, əvəzetmə reaksiyalarına daxil olur, üçlü amin xassəsi göstərir, tsikl açıla bilir.
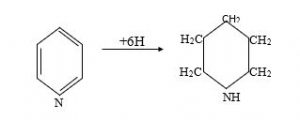
I. Özünəbirləşdirmə reaksiyaları. Benzoldan fərqli olaraq piridin hidrogenin ayrılma anında (Na + C2H5OH) reduksiya olunaraq piperidin əmələ gətirir.
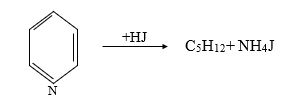
Benzol 2800C temperaturda HJ turşusu ilə metiltsiklopentan verdiyi halda, oxşar şəraitdə piridin n-pentan və ammonium yodid verir:
Benzol katalitik hidrogenləşmədə (180 0C) tsikloheksan, piridin isə amilamin verir. Belə ki, bundan əvvəlki halda olduğu kimi piridin həlqəsi sınır:
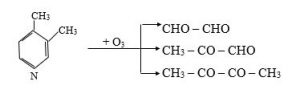
Piridinin ozonolizi də benzola nisbətən çətin gedir. 3,4-Dimetilpiridinin ozonolizindən qlioksal, metilqlioksal və diasetil alınır:
A. Elektrofil əvəzlənmə. Piridin elektrofil əvəzlənməyə az meyillidir. Azot atomu həlqənin elektron sıxlığını azaldır, çünki karbona nisbətən azot daha güclü elektromənfidir. Bundan başqa elektrofil reagentlər ilk növbədə azot atomuna həmlə edərək onda elektromüsbət mərkəz yaradır. Ona görə də əmələ gələn σ-kompleksi verilmiş halda molekulada ikinci elektromüsbət mərkəzin yaranmasını zəruri edir ki, bunun da ehtimalı azdır. β-Vəziyyətdə olan σ-kompleksi daha stabildir, çünki onun rezonans stabilliyi azot atomunda yaranan, ikinci müsbət yüklə əlaqəsi yoxdur.
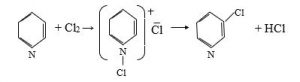
1. Aşağı temperaturda halogenlər piridinə birləşərək N-halogenidlər əmələ gətirir ki, onlar da qızdırıldıqda β-piridinhalogenidlərə çevrilir:
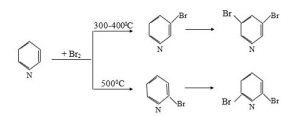
Katalizator olmadan 300-400 0C temperaturda əvəzlənmə ancaq 3 və 5-vəziyyətində gedir. Piridin 500 0C-də bromlaşması yumşaq gedərək α-vəziyyətdə (2 və 6) əvəzlənmə məhsulları əmələ gəlir:
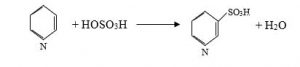
2. Qatı sulfat turşusu ilə piridini civə sulfat iştirakı ilə 24 saat müddətində 220-230 0C temperatura qədər qızdırdıqda piridin-3-sulfoturşu əmələ gəlir. Civə katalizatoru olmadan reaksiya 300 0C-də gedir və az çıxımla piridin-3-sulfoturşu alınır:
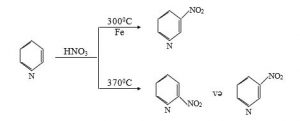
3. Piridinin nitrolaşması da sərt şərait tələb edir. Nitrat turşusunda kalium nitrat məhluluna dəmir katalizatoru və 300 0C-də 100%-li H2SO4 turşusunda piridin məhlulu ilə təsir etdikdə 22% çıxımla 3-nitropiridin alınır. 370 0C-də reaksiya aparıldıqda da yenə 2-nitropiridin əmələ gəlir:
Daha yumşaq şəraitdə nitrolaşma getmir.
B. Nukleofil əvəzlənmə. Piridin həlqəsində elektron sıxlığının zəifləməsi nəticəsində elektrofil əvəzlənmə çətinləşdiyi halda, nukleofil əvəzlənmə asanlaşır. Benzoldan fərqli olaraq piridin nukleofil reagentlərlə asan reaksiyaya daxil olur, eyni zamanda həmlə α və ya γ-vəziyyətlərində baş verir. Göstərilən vəziyyətlərdə σ-kompleksi asan əmələ gəlir, belə ki, onların rezonans stabilləşməsi mənfi yükün yaranması ilə əlaqəsi yoxdur.
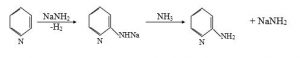
1. Piridini NaNH2 (natrium amid) ilə qızdırdıqda α-amino- piridin əmələ gəlir (A. E. Çiçibabin reaksiyası):
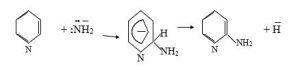
Bu reaksiya maye ammonyak mühitində daha yaxşı gedir və mexanizmi aşağıdakı kimidir:
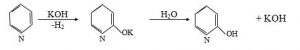
2. Quru kalium qələvisinə 250-3000C-də piridin buxarları ilə təsir etdikdə α-oksipiridin alınır (A. E. Çiçibabin):
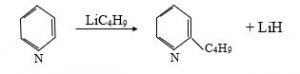
3. Bir sıra nukleofil reaksiyaları da məlumdur ki, burada aktiv reagent karbaniondur. Məsələn, butillitium piridini α-vəziyyətdə alkilləşdirir:
V. Radikal əvəzlənmə. Diazonium duzunun sulu məhluluna (C6H5N2Cl) artıqlaması ilə götürülmüş piridinlə təsir etdikdə α, β və γ – arilpiridin alınır:
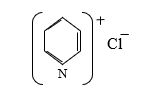
III. Piridinin üçlü amin kimi reaksiyaları. Piridin və onun homoloqları zəif əsasi xassə göstərir. Onlar HCl, HBr, H2SO4 turşuları ilə duz əmələ gətirir:
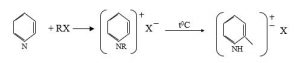
Üçlü amin kimi piridin asanlıqla alkilhalogenidləri birləşdirərək alkilathalogenidlər əmələ gətirir:
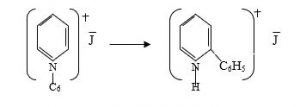
Alkilathalogenidləri qızdırdıqda alkil radikalı azot atomundan nüvənin α və ya –vəziyyətlərdəki karbon atomuna (2 və ya 4) keçir (β-vəziyyətə deyil). Məsələn, piridinin etilyodu izomerləşərək 2-etilpiridinyodidə çevrilir:
Sirkə turşusu məhlulunda piridini hidrogen-peroksidlə işlədikdə N-oksid əmələ gəlir:
Piridinə nisbətən piridinin N-oksidi elektrofil əvəzlənməyə daha meyillidir.
Piridin SO3 ilə C5H5N∙SO3 birləşməsi əmələ gətirir ki, ondan da pirrolun və s. sulfolaşmasında istifadə edirlər.
IV. Piridin həlqəsinin açılması. Piridin benzoldan həlqənin asan açılmasına görə kəskin fərqlənir. Yuxarıda bu reaksiyalara baxılmışdır.
Ayrı-ayrı nümayəndələri. Tətbiqi.
Piridin kəskin iyli rəngsiz mayedir; 115,3 0C-də qaynayır, sıxlığı 0,9772-dir. Su ilə maksimum sıxlıqlı qarışıq verir. Su ilə qarışdıqda həcminin azalması və istiliyin ayrılması piridinin hidrat birləşməsinin əmələ gəlməsini göstərir. Piridindən həlledici və katalizator kimi üzvi sintez reaksiyalarında istifadə olunur.
Piridin karbon turşuları
Piridin sırası karbon turşularını piridinin homoloqlarını oksidləşdirməklə, həmçinin bəzi alkaloidlərdən və xinolinin törəmələrindən alırlar.
α-Piridinkarbon turşusu pikolin, β-piridinkarbon turşusu nikotin və γ-piridinkarbonturşusu isə izonikotin turşusu adlanır. Bu turşular bərk maddələr olub, amfoter xarakterə malikdir. Zəif əsasi xassəyə malikdirlər. Α-Turşular asan dekarboksilləşir, β- və γ-turşular isə piridinə və CO2-yə parçalanır (əhənglə qızdırıldıqda).
Piridin sıra turşuları bir çox hallarda aromatik turşulara oxşardır. Onlar da xloranhidrid, efir, amid və s. əmələ gətirir. β-Piridinkarbon turşusunu (nikotin turşusu) nikotini və anabazini nitrat turşusu ilə oksidləşdirməklə alırlar. O, təbiətdə geniş yayılmışdır: qara ciyərdə, mayanın ekstraktında, süddə, dəndə olur. PP vitamini adı altında tətbiq olunur.
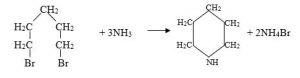
Piperidin C5H11N. Piperidinin quruluşunu onun 1,5-dibrompentana ammonyakla təsir reaksiyası da təsdiq edir:
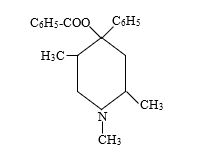
Rəngsiz mayedir; 105,6 0C-də qaynayır, su ilə qarışır. Tsikloheksan kimi piperidin «kreslo»ya bənzər konformasiyaya malikdir. Piperidin alifatik aminlərə xas olan xassələr daşıyır. Piperidinə nisbətən qüvvətli əsasi xassə göstərir. Oksidləşdiricilərin təsirinə qarşı davamlıdır. Piperidinin ən mühüm törəməsi ağrıkəsici dərman maddəsi olan promedoldur. Onu ilk dəfə İ. N. Nazarov almışdır. Quruluşu aşağıdakı kimidir:
Ədəbiyyat:
- Органическая химия, К. Д. Ненницеску, Москва, 1963
- Органическая химия, Л. Физер, М. Физер. Москва,1969
- Məhərrəmov A. M., Allahverdiyev M. Ə., Üzvi kimya, Bakı-2007